近日,浙江大学医学院附属第一医院精神卫生中心黄满丽教授团队与杭州师范大学/全省精神障碍精准诊疗重点实验
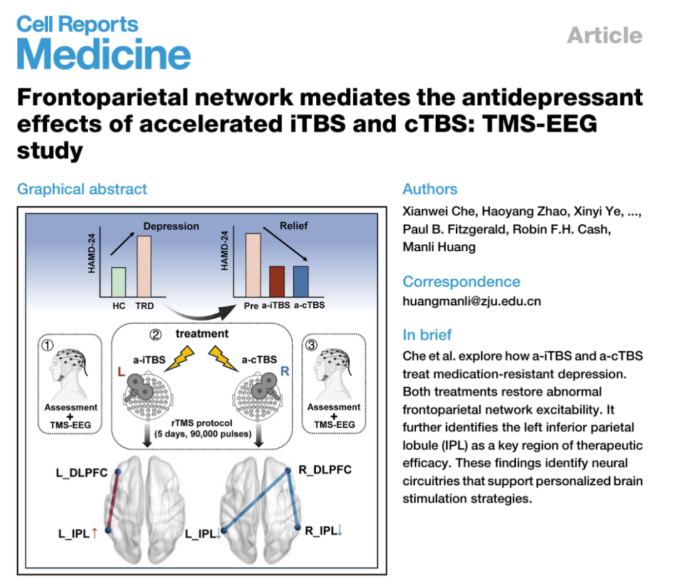
室车先伟副教授联合在《Cell Report Medicine》(IF=10.6)杂志上发表了题为“Frontoparietal network mediates the
antidepressant effects of accelerated iTBS and cTBS: TMS-EEG study”的研究论文。该研究在国际上首次揭示了在难治
性抑郁症患者中两种加速θ爆发脉冲刺激模式(accelerated theta burst stimulation, a-TBS)发挥抗抑郁作用的额顶网络
神经可塑性机制,提供了支持个性化神经调控策略的神经回路。
难治性抑郁症(TRD)指对至少两种足量足疗程抗抑郁治疗反应不佳的抑郁状态,约占抑郁症患者的44%,具有症状
迁延、功能损害重、自杀风险高等特点,给患者、家庭及社会带来沉重负担。神经调控已成为TRD的重要治疗手段。近
年来,加速θ爆发脉冲刺激(a-TBS)模式通过缩短治疗周期、提高刺激频率,已展现出显著疗效,但其抗抑郁作用的神
经机制尚不明确。
本研究首次采用同步经颅磁刺激-脑电图(concurrent TMS and electroencephalography, TMS-EEG)技术,在40名
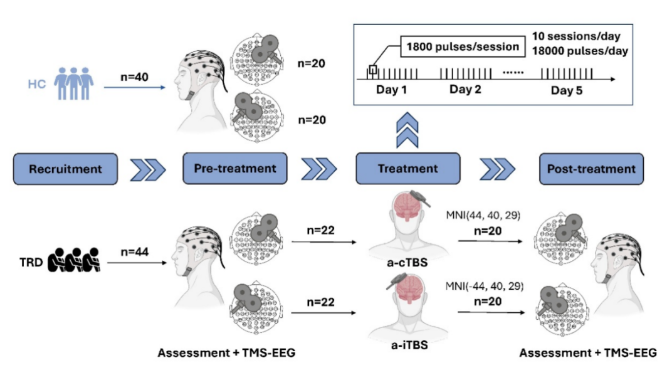
TRD患者与40名健康对照中,系统探究了两种加速TBS模式——加速间歇性TBS(a-iTBS)(简化斯坦福模式)与加速连
续性TBS(a-cTBS)(团队国际首创模式)——的神经可塑性机制(治疗方案见下图)。研究不仅刻画了TRD患者大脑局
部兴奋性与网络连接的异常特征,更揭示了a-iTBS与a-cTBS通过差异化调控额顶网络实现抗抑郁作用的共同通路。
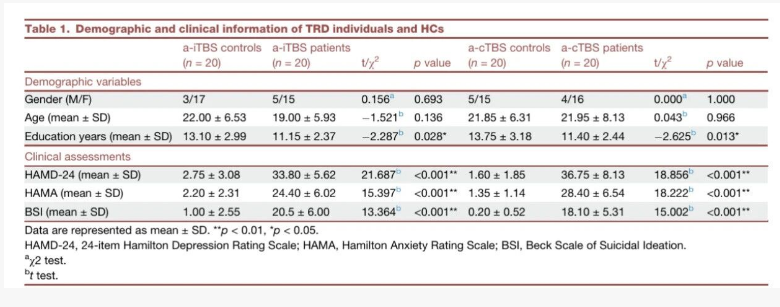
临床资料表明,TRD患者和健康对照在年龄和性别方面均无统计学差异,TRD 患者的教育年数略少于健康研究组
(a-iTBS:11.15 年vs 13.10 年;a-cTBS:11.40 年vs 13.75 年)。TRD患者的抑郁、焦虑、自杀意念的评分远高于健康对
照。(表1)
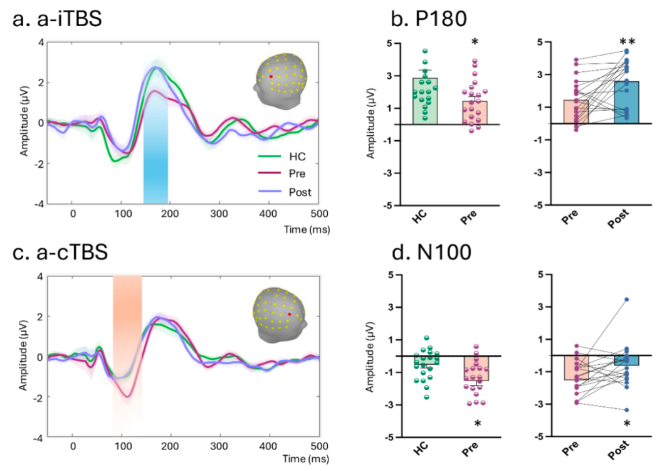
通过计算TMS诱发电位(TMS-evoked potentials, TEPs)来测量局部兴奋性改变。结果显示,TRD患者在左侧背外侧前
额叶(DLPFC)表现为低兴奋性(P180波幅降低),在右侧DLPFC则表现为抑制功能不足(N100波幅过度负向)。
a-iTBS治疗后左侧P180波幅升高,a-cTBS治疗后右侧N100波幅恢复正常,提示两种治疗分别通过对左右半球兴奋 / 抑制
平衡的调节发挥治疗作用。(见下图)
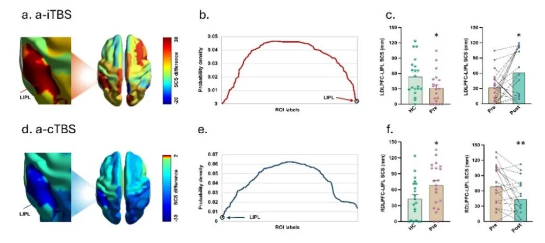
通过显著电流散射(Significant current scattering, SCS) 和显著电流密度(significant current density, SCD)两个指标
反映额顶网络连接的重塑。计算SCS发现,a-iTBS治疗后,增强了TRD患者从左侧背外侧前额叶(DLPFC)到左侧顶下
小叶(IPL) 的电流传播,提升该网络连接强度。而a-cTBS治疗后降低了从右侧DLPFC到左侧IPL 的过度电流传播,抑
制异常网络活动。二者均使TRD患者异常的额顶网络连接趋向健康对照水平。(见下图)
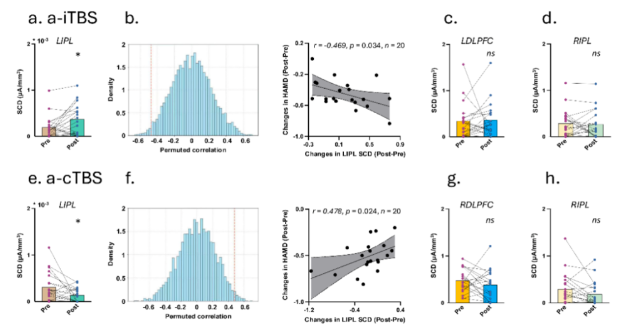
计算SCD发现,a-iTBS治疗后,左侧IPL的电流密度显著增加,且增加幅度与抑郁症状改善程度正相关。a-cTBS治疗
后,左侧IPL的电流密度显著降低,降低幅度也与症状改善相关。这表明左侧顶下小叶(IPL)可能是两种不同TBS模式
发挥抗抑郁作用的关键节点。(见下图)
综上所述,该研究通过高时空分辨率的TMS-EEG技术,揭示了加速TBS治疗难治性抑郁症的额顶网络机制,其中加
速iTBS增加了左侧兴奋性,增加了左侧DLPFC至左侧IPL的连通性;加速cTBS模式对右侧皮质有广泛抑制,降低了右侧
DLPFC至左侧IPL的连通性。本研究为探索难治性抑郁症的神经可塑性机制以及发展精准、高效的加速神经调控策略奠定
了重要理论基础,未来,结合脑网络特征为患者个体化定制TBS治疗方案,有望进一步提升难治性抑郁症的临床应答率与
治愈率。
浙大一院黄满丽教授为唯一通讯作者; 杭州师范大学/全省精神障碍精准诊疗重点实验室车先伟副教授、浙大一院精卫
中心23级博士生赵昊阳和21级八年制博士生叶欣怡为共同第一作者。本研究还得到了浙大一院胡少华教授、中国科学院心
理研究所的胡理教授和涂毅恒教授、澳大利亚国立大学的Paul Fitzgerald教授、墨尔本大学Robin Cash教授、莫纳什大学
Bernadette Fitzgibbon的大力支持。感谢所有参与研究的受试者。该研究由国家自然科学基金(82271562)、浙江省重点
研发计划(2023C03077)和浙江省自然科学基金(LQ22H090005、LY23C090002)和全省精神障碍精准诊疗重点实验室
开放研究基金(2025A2)资助完成。
参考文献
Che X, Zhao H, Ye X, Ye S, Zhen Z, Huang Z, Li Y, Zhang S, Xu P, Chen X, Jiang C, Pan F, Luan H, Chen J,
Shang D, Hu S, Tu Y, Hu L, Fitzgibbon BM, Fitzgerald PB, Cash RFH, *Huang M. Frontoparietal network mediates the
antidepressant effects of accelerated iTBS and cTBS: TMS-EEG study. Cell Rep Med. 2025 Dec 3:102470.
doi: 10.1016/j.xcrm.2025.102470. Epub ahead of print. PMID: 41344323.